Navigation auf uzh.ch
Navigation auf uzh.ch
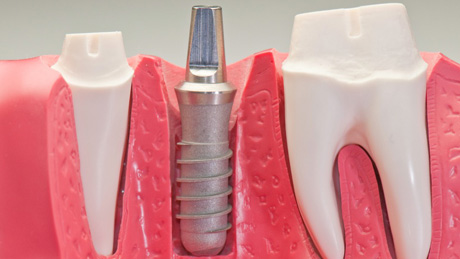
Die Vorstellung, dass einem Patienten Strom auf die Titanschraube seines Zahnimplantats geleitet wird, lässt einen erschaudern. Folter? Nein. Die richtige Dosis Strom lässt Bakterien absterben. Wenige Milliampere, die der Patient je nach Sensibilität und Stromstärke entweder gar nicht oder als leichte Muskelkontraktion wahrnimmt, reichen dafür aus.
Dieses Resultat zeigten die Experimente, die Dirk Mohn im Rahmen seiner Doktorarbeit bei ETH-Professor Wendelin Stark vom Institut für Chemie- und Bioingenieurwissenschaften in Zusammenarbeit mit Thomas Imfeld, Professor für Präventivmedizin, Parodontologie und Kariologie am Zentrum für Zahnmedizin der Universität Zürich, durchgeführt hat.
In den letzten zehn Jahren hat sich die Zahl der eingesetzten Zahnimplantate in Europa und den USA verdoppelt. «In den industrialisierten Ländern wurden im Jahr 2009 schätzungsweise fünf Millionen Zahnimplantate eingesetzt, davon etwa eine Million in Deutschland und 100'000 in der Schweiz», sagt Thomas Imfeld.
Parallel dazu habe sich seit 1994 auch die Anzahl der Zahnärzte verdoppelt, die Implantate setzen. Heute würden 80 Prozent der Zahnärzte in der Schweiz derartige Eingriffe vornehmen, davon jedoch nur 30 Prozent regelmässig, dass heisst mehr als 50 Implantierungen pro Jahr, betont der Zahnmediziner. Bei rund zehn Prozent der Implantate treten Probleme auf, meist im ersten Jahr nach dem Eingriff. Das Implantat heilt erst gar nicht im Knochen ein, oder das Gewebe rund um ein Implantat infiziert sich. Eine solche Infektion kann schliesslich bis zum Knochenschwund führen und dazu, dass das Implantat wieder entfernt werden muss.
Die Behandlung sogenannter peri-implantärer Entzündungen erfolgt heute mechanisch mit Abrasiv- oder Laser-Verfahren oder mit lokal angewendeten Antibiotika. Ziel der Forscher war es, ein nicht invasives Verfahren zu entwickeln, um solche Entzündungen effizient und schonend zu behandeln. «Die Idee stammt aus der Wasserreinigung, wo mit Hilfe von Strom eine klassische Elektrolyse erzeugt wird», sagt Dirk Mohn. Ein mit physiologischer Kochsalzlösung hergestelltes Gelatinepräparat nutzen die Wissenschaftler als Kieferersatz. In dieses platzieren sie original Titanium-Implantate, die sie zuvor mit einem Bakterienfilm aus Escherichia Coli-Bakterien beschichteten.
Im Experiment dient für den Stromfluss ein Implantat als Kathode und eines als Anode. Die Implantate werden während 15 Minuten Stromstärken zwischen 0 und 10 Milliampere ausgesetzt. Die durch das erzeugte Spannungsfeld verursachte Elektrolyse führte dazu, dass Wassermoleküle an der Kathode in Hydroxid-Ionen zerlegt werden und somit der pH-Wert steigt. Farbindikatoren in der Gelatine zeigen das alkalische Milieu durch einen Farbumschlag an. An der Anode hingegen sinkt der pH-Wert und aus der Kochsalzlösung entstehen stark oxydative Substanzen wie Chlor.
Oxydative Chlorspezies sind die Schlüsselkomponenten der elektrochemischen Reaktion, denn diese Substanzen haben eine viel höher desinfizierende Wirkung als das rein alkalische Milieu an der Kathode. Die Versuchsreihen mit unterschiedlichen Stromstärken zeigen, dass bei den als Anode fungierenden Implantaten nach einer fünfzehnminütigen Behandlung mit einer Stromstärke von weniger als zehn Milliampere 99 Prozent der Bakterien abgetötet werden.
Beim Patienten würde deshalb das Implantat die Funktion der Anode übernehmen. Denkbar wäre ein Clip an der Lippe als Kathode, sagt Mohn. Momentan sind die Wissenschaftler dabei ein entsprechendes Gerät für erste Versuche am lebenden Organismus – etwa an Hunden – zu entwickeln. Parallel dazu erweitern die Wissenschaftler ihre in vitro Versuchsanordnung mit einer breiteren Bakterienpopulation, die der Bakterienvielfalt im Mund entspricht.